Transferts couplés de biochaleur
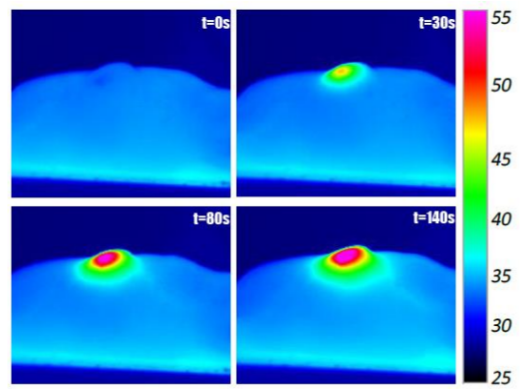
injectée de nanotubes est soumise à un laser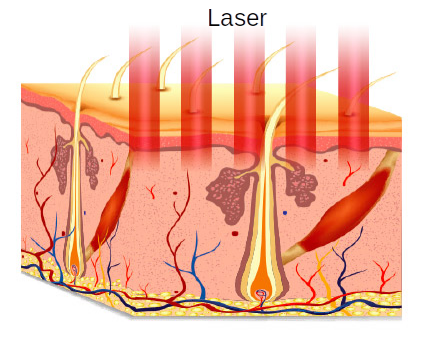

Dès leur naissance en 1960, les lasers sont apparus comme des sources de lumière potentiellement intéressantes pour la médecine car elles avaient trois caractéristiques qui les distinguaient des sources conventionnelles : la directivité, la possibilité de fonctionner en mode pulsé, et la monochromaticité. L’hyperthermie induite par laser est un type de traitement du cancer dans lequel les tissus de l’organisme sont exposés à des températures élevées pour endommager et tuer les cellules cancéreuses. Une meilleure compréhension de ce processus par la voie de la modélisation et de la simulation numérique permettrait d’améliorer l’efficacité de ce type de traitement afin de se rapprocher de l’efficacité de traitement plus conventionnel tel que la chimiothérapie. La problématique rencontrée par le milieu médical lorsque l’on s’intéresse au traitement par hyperthermie concerne plus spécifiquement la définition des paramètres opératoires (puissance, fréquence de pulse, zone à cibler, longueur d’onde du laser). Travaillant originellement sur le diagnostic du cancer par TOD (Tomographie Optique Diffuse)[1], l’équipe «Rayonnement dans les tissus biologiques» du LEMTA mène actuellement des recherches visant à apporter des réponses précises à ces questions.
La soumission de biologiques à un éclairement plus ou moins intense associé à des temps de pulse de l’ordre de la milliseconde induit des effets photothermiques au sein de ces tissus. La conversion de la lumière en chaleur engendre une source primaire de chaleur au sein du milieu. Un transfert de chaleur aboutit alors à un volume chauffé plus volumineux. La connaissance de ce volume chauffé secondaire est déterminante pour l’étude de sa dénaturation tissulaire (réaction chimique de dégradation des tissus). L’effet de coagulation, souhaité dans le cadre du traitement de manifestations tumorales, se produit pour des températures comprises entre 50°C et 99°C. La compréhension des phénomènes associés à ce processus de dénaturation est une des clés de la lutte contre le cancer. Du point de vue de la modélisation, ce processus est généralement évalué à travers un taux d’endommagement tissulaire ayant la forme d’une loi d’Arrhenius fortement non linéaire couplée à la température. Les travaux actuels visent à étudier les phénomènes physiques mis en jeu dans un tissu biologique lorsque l’on souhaite éliminer une tumeur par l’exposition au laser. Le développement d’un modèle fin des transferts de «bio-chaleur» rendant compte de la complexité des matrices biologiques permettra une meilleure compréhension du mécanisme de dénaturation tissulaire des tumeurs cancéreuses.
Les verrous scientifiques identifiés portent sur une modélisation fine des transferts de «bio-chaleur» au sein du milieu vivant, identifiée comme une première étape fondamentale. La complexité du milieu biologique (milieu très hétérogène, poreux et vascularisé, production de chaleur métabolique) se combine avec les différents modes de transfert de chaleur (rayonnement, conduction, convection) à considérer afin de rendre fidèlement compte des variations de température aux petites échelles de temps.
Références